Göttinger Wissenschaftler entschlüsseln am BESSY II grundlegende Wirkprinzipien biochemischer Reaktionen
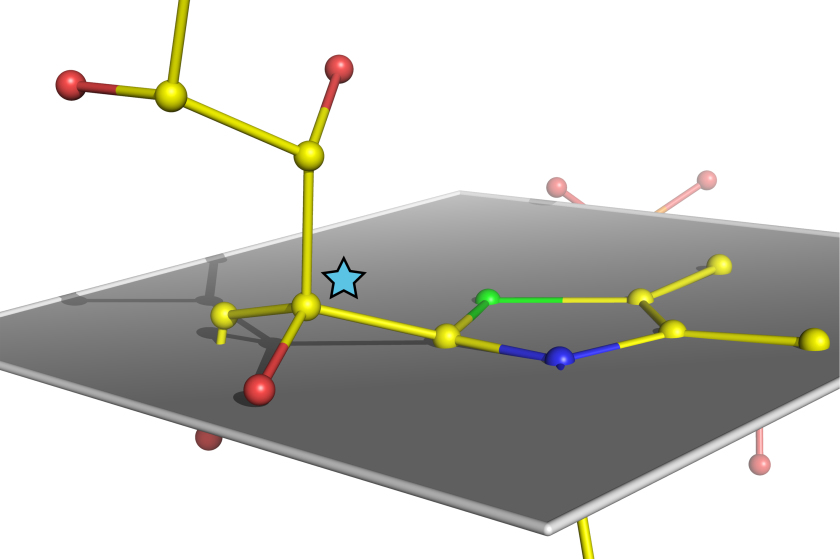
Atomare Struktur eines verbogenen, kurz vor der Spaltung stehenden Zuckermoleküls im humanen Enzym Transketolase.
Enzyme sind die molekularen Katalysatoren des Lebens mit vitalen Funktionen im Stoffwechsel jeder Zelle. Bisher wurde spekuliert, dass Enzyme bei der Durchführung biochemischer Reaktionen ihre Ausgangsstoffe regelrecht verbiegen und dadurch spalten können. Wissenschaftlern am Göttinger Zentrum für Molekulare Biowissenschaften (GZMB) ist es nun erstmals gelungen, diese Hypothese zweifelsfrei zu bestätigen. Dazu nutzten sie die MX-Beamline an BESSY II. Die Ergebnisse der Studie sind in der renommierten Fachzeitschrift Nature Chemistry erschienen.
Die Göttinger Wissenschaftler unter der Leitung von Prof. Dr. Kai Tittmann und Prof. Dr. Ralf Ficner züchteten zunächst hochgeordnete Proteinkristalle des humanen Enzyms Transketolase, das eine Schlüsselrolle bei der Verwertung von Zuckern im menschlichen Stoffwechsel einnimmt. Diese Proteinkristalle versetzten sie mit den natürlichen Zuckersubstraten. Die Analyse der Struktur des Enzymkristalls erfolgte anschließend an der MX-Beamline des Elektronenspeicherrings BESSY II und im französischen Grenoble. Den Wissenschaftlern gelang es, eine ultrahochaufgelöste Struktur des im Enzym gebundenen Zuckermoleküls unmittelbar vor seiner Spaltung in zwei Teile, mit einer extrem hohen Ortsauflösung von 0,1 Nanometer zu bestimmen. „Dieser in seiner Schärfe bis heute einmalige Schnappschuss eines arbeitenden Enzyms offenbart unzweifelhaft, dass das Zuckersubstrat im Enzym verbogen wird wie ein eingespanntes Werkstück in einem Schraubstock“, sagt Prof. Tittmann.
Enzyme stellen oft Angriffspunkte für Medikamente dar. Deshalb sind die neuen Erkenntnisse wichtig für die Entwicklung maßgeschneiderter, hochspezifischer Wirkstoffe, wie zum Beispiel für die Krebstherapie. „Auch die in der vorliegenden Studie untersuchte humane Transketolase übt eine Schlüsselfunktion im Stoffwechsel von Krebszellen aus“, sagt Prof. Tittmann.
Quelle: Universität Göttingen
https://www.helmholtz-berlin.de/pubbin/news_seite?nid=13800;sprache=deamp
- Link kopieren
-
BESSY II: Eingebauter Sauerstoff verkürzt die Lebensdauer von Feststoffbatterien
Feststoffbatterien sind sicher und leistungstark, aber ihre Kapazität nimmt zurzeit noch rasch ab. Ein Team der TU Wien, der Humboldt-Universität zu Berlin und des HZB hat nun eine TiS₂|Li₃YCl₆-Halbzelle an BESSY II analysiert. Dafür nutzte das Team eine spezielle Probenumgebung, die eine zerstörungsfreie Untersuchung unter realen Betriebsbedingungen ermöglicht. Durch die Kombination von Weich- und Hart-Röntgen-Photoelektronenspektroskopie (XPS und HAXPES) konnte ein neuer Degradationsmechanismus identifiziert werden. Dabei spielte das Element Sauerstoff eine besondere Rolle. Die Studie liefert wertvolle Einblicke, um Design und Fertigung von Feststoffbatterien zu verbessern.
-
Spintronik an BESSY II: Echtzeit-Analyse von magnetischen Doppelschichtsystemen
Spintronische Bauelemente ermöglichen Datenverarbeitung mit deutlich weniger Energieverbrauch. Sie basieren auf der Wechselwirkung zwischen ferromagnetischen und antiferromagnetischen Schichten. Nun ist es einem Team von Freier Universität Berlin, HZB und Universität Uppsala gelungen, für jede Schicht separat zu verfolgen, wie sich die magnetische Ordnung verändert, nachdem ein kurzer Laserpuls das System angeregt hat. Dabei konnten sie auch die Hauptursache identifizieren, die für den Verlust der antiferromagnetischen Ordnung in der Oxidschicht sorgt: Die Anregung wird von den heißen Elektronen im ferromagnetischen Metall zu den Spins im Antiferromagneten transportiert.
-
Umweltchemie an BESSY II: Radikale in Gewässern
Wie entstehen in wässrigen Lösungen unter UV-Licht so genannte Radikale? Diese Frage spielt sowohl für die Gesundheitsforschung als auch für den Umweltschutz eine wichtige Rolle, beispielsweise im Zusammenhang mit der Überdüngung von Gewässern durch die Landwirtschaft. Ein Team hat nun an BESSY II eine neue Methode etabliert, um Hydroxyl-Radikale in Lösung zu untersuchen. Mit einem Trick konnten sie überraschende Einblicke in den Reaktionspfad gewinnen.
