4000. Proteinstruktur an BESSY II entschlüsselt
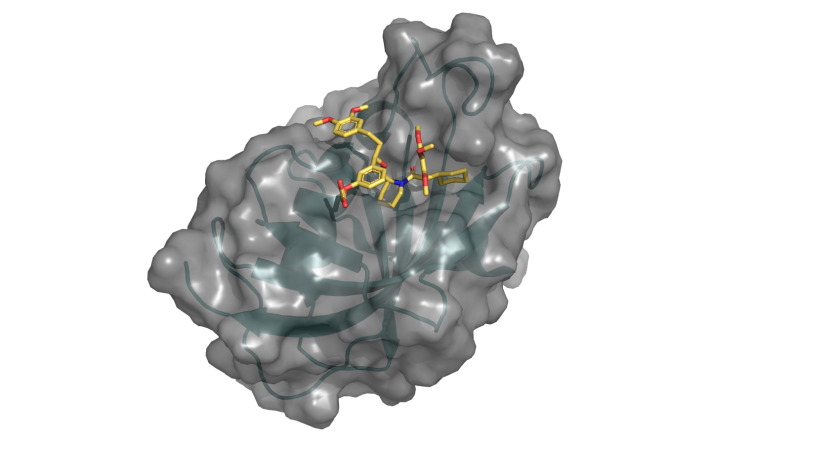
Die 4000. Proteinstruktur aus dem HZB BESSY, die in der PDB veröffentlicht wurde, zeigt die G64S-Variante von FKBP51 im Komplex mit dem hochselektiven Liganden SAFit (eingezeichnete Struktur). © C. Meyners/TU Darmstadt/HZB
Bei der 4000. Struktur handelt es sich um das Molekül FKBP51, das mit stressinduzierten Erkrankungen wie Depressionen, chronischen Schmerzen und Diabetes zusammenhängt. Das Team um Prof. Dr. Felix Hausch, TU Darmstadt, nutzt die Kenntnis der dreidimensionalen Struktur, um neue Strategien für das Design passender Medikamente zu entwickeln.
Viele Erkrankungen hängen mit Fehlfunktionen von Proteinen im Organismus zusammen. Die dreidimensionale Architektur dieser Moleküle ist oft äußerst komplex, liefert aber wertvolle Hinweise, wie sich die Fehlfunktion beheben ließe, beispielsweise durch Medikamente, die sich perfekt in eine „Tasche“ an das Zielmolekül binden und die Fehlfunktion blockieren. Die Struktur von Proteinen lässt sich mit Röntgenanalysen an den MX-Beamlines von BESSY II entschlüsseln.
In der Protein Data Bank (www.rcsb.org/pdb), die alle experimentell bestimmten Proteinstrukturen enthält, ist nun die 4000. Struktur aus BESSY II eingetragen worden. Das Team um Prof. Felix Hausch von der TU Darmstadt hatte Proteinkristalle aus dem Molekül FKBP51 hergestellt und an den MX-Beamlines untersucht.
Dabei handelt es sich um ein Protein, das eine besondere Rolle bei den großen Gesundheitsproblemen unserer Zeit spielt. Denn FKBP51 reguliert die Signaltransduktion von Steroidhormonrezeptoren, die durch Stress gestört sein kann. Dies kann Depressionen, chronische Schmerzen oder Krankheiten wie Diabetes und Übergewicht auslösen. Das Protein FKBP51 hat sich als vielversprechender Angriffspunkt für Medikamente gegen diese Krankheiten erwiesen. „Die Proteinstrukturanalyse zeigt uns, wo im Molekül interessante „Taschen“ sitzen, die als Zielpunkte für Medikamente in Frage kommen“, sagt Dr. Christian Meyners, TU Darmstadt.
arö
https://www.helmholtz-berlin.de/pubbin/news_seite?nid=24367;sprache=de/
- Link kopieren
-
Proteinkristallographie an BESSY II: Schneller, besser und automatischer
Viele Erkrankungen hängen mit Fehlfunktionen von Proteinen im Organismus zusammen. Die dreidimensionale Architektur dieser Moleküle ist oft äußerst komplex, liefert aber wertvolle Hinweise für das Verständnis von biologischen Prozessen und die Entwicklung von Medikamenten. Mit Röntgendiffraktion an den MX-Beamlines von BESSY II lässt sich die 3D Struktur von Proteinen entschlüsseln. Mehr als 5000 Strukturen sind bis heute an den drei MX-Beamlines von BESSY II gelöst worden. Ein Rückblick und Ausblick im Gespräch mit Manfred Weiss, dem Leiter der Makromolekularen Kristallographie.
-
5000. Proteinstruktur an BESSY II: Startpunkt für einen COVID-Wirkstoff
Viele Proteine besitzen eine komplexe Architektur, die bestimmte biologische Funktionen ermöglicht. An manchen Stellen können Moleküle andocken und die Funktion des Proteins verändern. Ein Team am HZB hat nun das Nsp1-Protein untersucht, das bei der Infektion mit dem SARS-CoV-2-Virus eine Rolle spielt. Sie analysierten Proteinkristalle, die sie zuvor mit Molekülen aus einer Fragmentbibliothek versetzt hatten und entdeckten dabei insgesamt 21 Kandidaten als Startpunkte für die Medikamentenentwicklung. Gleichzeitig entschlüsselten sie damit auch die 5000. Struktur an BESSY II.
-
Was die Zinkkonzentration in Zähnen verrät
Zähne sind Verbundstrukturen aus Mineralien und Proteinen, dabei besteht der Großteil des Zahns aus Dentin, einem knochenartigen, hochporösen Material. Diese Struktur macht Zähne sowohl stark als auch empfindlich. Neben Kalzium und Phosphat enthalten Zähne auch Spurenelemente wie Zink. Mit komplementären mikroskopischen Verfahren hat ein Team der Charité Berlin, der TU Berlin und des HZB die Verteilung von natürlichem Zink im Zahn ermittelt. Das Ergebnis: mit zunehmender Porosität des Dentins in Richtung Pulpa steigt die Zinkkonzentration um das 5- bis 10-fache. Diese Erkenntnis hilft, den Einfluss von zinkhaltigen Füllungen auf die Zahngesundheit besser zu verstehen und könnte Verbesserungen in der Zahnmedizin anstoßen.
