Neuer Detektor beschleunigt die Proteinkristallographie
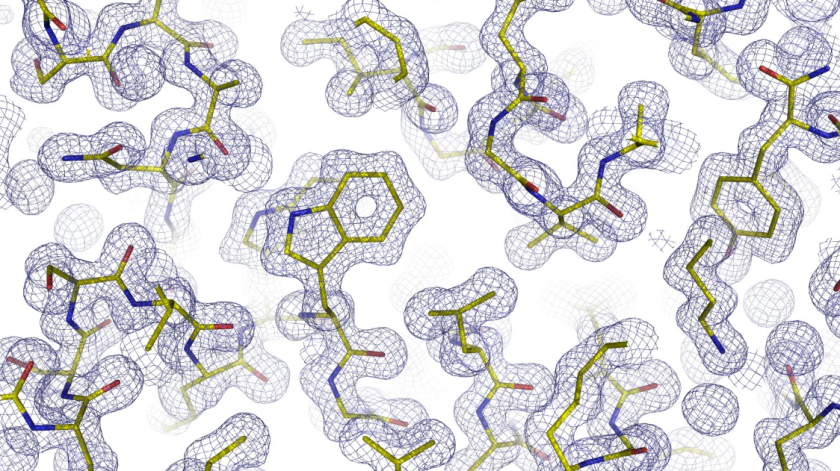
Nur 60 Sek. Messzeit mit dem neuen Detektor reichten schon aus, um die Elektrondichte des PETase-Enzyms zu ermitteln. Sie zeigt alle strukturellen Merkmale des Enzyms. © HZB

Der neue PILATUS-Detektor wurde an der MX-Beamline 14.1 in Betrieb genommen. © HZB
An einer der drei MX-Beamlines am HZB wurde letzte Woche ein neuer Detektor installiert. Im Vergleich zum alten Detektor ist der neue besser, schneller und empfindlicher. Er ermöglicht es, binnen kürzester Zeit vollständige Datensätze von komplexen Proteinen aufzunehmen.
Proteine bestehen aus tausenden von Bausteinen, die komplexe Architekturen mit gefalteten oder verwickelten Bereichen bilden können. Für die Funktion des Proteins im Organismus spielt ihre Gestalt jedoch die entscheidende Rolle. Mit Hilfe der makromolekularen Kristallographie an BESSY II ist es möglich, die Architektur von Proteinmolekülen zu entschlüsseln. Dafür werden winzige Proteinkristalle mit Röntgenlicht aus der Synchrotronquelle BESSY II durchleuchtet. Aus den gewonnenen Beugungsmustern lässt sich die Morphologie der Moleküle errechnen.
Nun hat das MX-Team an BESSY II an der MX-Beamline 14.1 einen neuen Detektor in Betrieb genommen, der zwei- bis dreimal schneller als bisher arbeitet. Als Probe analysierte das Team einen Kristall aus dem Enzym PETase. PETase ist in der Lage, den Kunststoff PET teilweise abzubauen. In weniger als einer Minute konnte der Detektor einen vollständigen Beugungsdatensatz aufzeichnen, der Daten aus einem Winkelbereich von 180 Grad umfasst. Der Datensatz besteht aus 1200 Bildern, die jeweils 45 Millisekunden lang der Röntgenstrahlung ausgesetzt waren. „Die resultierende Elektronendichte war von ausgezeichneter Qualität und zeigte alle strukturellen Merkmale des Enzyms“, erklärt Dr. Manfred Weiss, der das MX-Team an BESSY II leitet.
Der Erfolg der HZB MX-Beamlines wird durch mehr als 3000 PDB-Einträge aus experimenteller Strahlzeit von mehr als hundert internationalen Nutzergruppen aus dem akademischen Bereich und pharmazeutischen Forschungsunternehmen dokumentiert.
red.
https://www.helmholtz-berlin.de/pubbin/news_seite?nid=21100;sprache=de
- Link kopieren
-
Magnon-Momentum-Mikroskopie: Neues Fenster in nanoskalige Spinwellen
Ein internationales Team unter der Leitung des Max-Born-Instituts hat eine neue Art der Momentum-Mikroskopie entwickelt, mit der Magnonen – die Quanten kollektiv angeregter Spins – mithilfe von Weichröntgenstrahlung direkt im zweidimensionalen reziproken Raum abgebildet werden können. Die Messungen fanden an BESSY II und Petra III statt. Erstautor ist der HZB-Physiker Steffen Wittrock. Dank ihrer Empfindlichkeit, Einfachheit und der Möglichkeit, Wellenlängen im Nanometerbereich aufzulösen, bildet diese neuartige Methode eine leistungsstarke und vielseitige Plattform für die Erforschung nichtlinearer Magnonen-Wechselwirkungen, die für zukünftige Rechenkonzepte interessant sind.
-
Magnetfeld während Katalysator-Synthese verdreifacht Ammoniakausbeute
Ein externes Magnetfeld während der Synthese von CoFe₂O₄-Dünnschichten verdreifacht beim Einsatz in der Elektrokatalyse die Ammoniakausbeute. Das Magnetfeld verändert die Oberflächenzustände der Spinell-Oxid-Dünnschichten, so dass die katalytisch aktiven Zentren stärker exponiert sind. Im Fachjournal 'Advanced Functional Materials' zeigt ein Team um Marcel Risch, HZB, und Sanjay Mathur, Universität Köln, eine skalierbare Strategie, um Elektrokatalysatoren der nächsten Generation für effiziente und nachhaltige chemische Umwandlungen zu entwickeln.
-
Materialchemie gestaltet die Zukunft der Katalyse
Die synthetische Materialchemie der Zukunft kann als Werkzeug dienen, um smarte und adaptive Elektrokatalysatoren zu entwickeln. Das Forschungsfeld entwickelt sich aktuell rasant, mit In-situ-Analytik, datengestützten Entdeckungen und autonomer Robotik. Diese neuen Ansätze könnten die Entdeckung langlebiger und effizienter Katalysatoren für die zukünftige Energieumwandlung und die Dekarbonisierung der chemischen Industrie beschleunigen. Einen Überblick bietet nun ein Beitrag aus dem Team des Katalyse-Experten Dr. Prashanth Menezes im renommierten Fachjournal Angewandte Chemie.
