IRIS-Beamline an BESSY II mit Nanomikroskopie erweitert
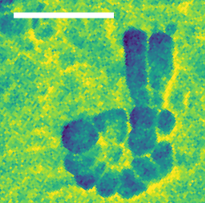
Infrarotabbildung des Nucleolus im Zellkern einer Fibroblastenzelle. Der Skalenstrich entspricht 500 Nanometern. © HZB
Die Infrarot-Beamline IRIS am Speicherring BESSY II bietet nun eine vierte Option, um Materialien, Zellen und sogar Moleküle auf verschiedenen Längenskalen zu charakterisieren. Das Team hat die IRIS-Beamline mit einer Endstation für Nanospektroskopie und Nanoimaging erweitert, die räumliche Auflösungen bis unter 30 Nanometer ermöglicht. Das Instrument steht auch externen Nutzergruppen zur Verfügung.
Die Infrarot Beamline IRIS am Speicherring BESSY II ist die einzige Infrarot-Beamline in Deutschland, die auch externen Nutzergruppen zur Verfügung steht und ist entsprechend stark nachgefragt. Dr. Ulrich Schade, der für die Beamline verantwortlich ist, entwickelt die Instrumente gemeinsam mit seinem Team weiter, um einzigartige, hochmoderne IR-Spektroskopie-Experimentiertechniken zu ermöglichen.
Im Rahmen eines kürzlich durchgeführten größeren Upgrades der Beamline errichtete das Team zusammen mit dem Institut für Chemie der HUB ein zusätzliches Infrarot-Nahfeldmikroskop (scattering-type scanning near-field optical microscope).
„Mit dem Nanoskop können wir Strukturen kleiner als ein Tausendstel des Haardurchmessers auflösen und kommen somit in Bereiche der innersten Strukturen von zum Beispiel biologischen Systemen, Katalysatoren, Polymeren und Quantenmaterialien“, sagt Dr. Alexander Veber, der diese Erweiterung durchgeführt hat.
Die neue Nanospektroskopie-Endstation basiert auf einem optischen Rastermikroskop und ermöglicht Bildgebung und Spektroskopie mit Infrarotlicht mit einer räumlichen Auflösung von mehr als 30 nm. Um die Leistungsfähigkeit der neuen Endstation zu demonstrieren, untersuchte Veber einzelne Zellulose-Mikrofibrillen und bildete Zellstrukturen ab. Alle Endstationen sind für nationale und internationale Nutzergruppen verfügbar.
Förderung: Bundesministerium für Bildung und Forschung [grant No. project 05K19KH1 (SyMS)]; Germany's Excellence Strategy (grant No. EXC 2008-390540038 – UniSysCat).
arö
https://www.helmholtz-berlin.de/pubbin/news_seite?nid=26746;sprache=de/
- Link kopieren
-
BESSY II: Eingebauter Sauerstoff verkürzt die Lebensdauer von Feststoffbatterien
Feststoffbatterien sind sicher und leistungstark, aber ihre Kapazität nimmt zurzeit noch rasch ab. Ein Team der TU Wien, der Humboldt-Universität zu Berlin und des HZB hat nun eine TiS₂|Li₃YCl₆-Halbzelle an BESSY II analysiert. Dafür nutzte das Team eine spezielle Probenumgebung, die eine zerstörungsfreie Untersuchung unter realen Betriebsbedingungen ermöglicht. Durch die Kombination von Weich- und Hart-Röntgen-Photoelektronenspektroskopie (XPS und HAXPES) konnte ein neuer Degradationsmechanismus identifiziert werden. Dabei spielte das Element Sauerstoff eine besondere Rolle. Die Studie liefert wertvolle Einblicke, um Design und Fertigung von Feststoffbatterien zu verbessern.
-
Spintronik an BESSY II: Echtzeit-Analyse von magnetischen Doppelschichtsystemen
Spintronische Bauelemente ermöglichen Datenverarbeitung mit deutlich weniger Energieverbrauch. Sie basieren auf der Wechselwirkung zwischen ferromagnetischen und antiferromagnetischen Schichten. Nun ist es einem Team von Freier Universität Berlin, HZB und Universität Uppsala gelungen, für jede Schicht separat zu verfolgen, wie sich die magnetische Ordnung verändert, nachdem ein kurzer Laserpuls das System angeregt hat. Dabei konnten sie auch die Hauptursache identifizieren, die für den Verlust der antiferromagnetischen Ordnung in der Oxidschicht sorgt: Die Anregung wird von den heißen Elektronen im ferromagnetischen Metall zu den Spins im Antiferromagneten transportiert.
-
Elektrokatalysatoren: Ladungstrennung an der Fest-Flüssig-Grenzfläche modelliert
Wasserstoff spielt für die Wende hin zur CO₂-Neutralität eine entscheidende Rolle, sowohl als Energieträger als auch als Ausgangsstoff für die grüne Chemie. Die großtechnische Erzeugung von Wasserstoff durch Elektrolyse sowie vieler anderer chemischer Produkte erfordert jedoch deutlich kostengünstigere und effizientere Katalysatoren. Um Elektrokatalysatoren gezielt zu verbessern, ist es von großem Nutzen, die elektrochemischen Prozesse genau zu verstehen, die an der Grenzfläche zwischen dem festen Katalysator und dem flüssigen Medium ablaufen. Ein europäisches Team hat In der Fachzeitschrift Nature Communications ein leistungsfähiges Modell vorgestellt, das die Ladungstrennung an der Grenzfläche, die Bildung der elektrischen Doppelschicht sowie deren Einfluss auf die katalytische Aktivität hervorragend beschreibt.
